Układ odporności
Spirulina Lipopolysaccharides Inhibit Tumor Growth
Source: Oncology Reports; Authors: Hiromi Okuyama Akira Tominaga, z Laboratory of Immunology, Faculty of Pharmacy, Osaka Ohtani University, Tondabayashi, Osaka 584-8540, Japan
Spirulina lipopolysaccharides inhibit tumor growth in a Toll-like receptor 4-dependent manner by altering the cytokine milieu from interleukin-17/interleukin-23 to interferon-γ
Spirulina lipopolysaccharides inhibit tumor growth in a Toll-like receptor 4-dependent manner by altering the cytokine milieu from interleukin-17/interleukin-23 to interferon-γ
Hiromi Okuyama Akira Tominaga Satoshi Fukuoka Takahiro Taguchi Yutaka Kusumoto Shiro Ono
Oncology Reports; 2017 Feb; 37(2): 684–694.
Abstract
Th17 cells and the cytokine they produce, interleukin (IL)-17, play an important role in tumor progression in humans and in mice. IL-6 and IL-23 are critical cytokines for the differentiation and propagation of Th17 cells, respectively. Bacterial lipopolysaccharides (LPS) are known to stimulate immune cells to produce such inflammatory cytokines. Contrary to Escherichia coli (E. coli) LPS, LPS from Spirulina has low toxicity and barely induces in vivo production of IL-6 and IL-23 in mice. We examined the antitumor effects of Spirulina LPS compared to E. coli LPS in an MH134 hepatoma model. Administration of Spirulina LPS suppressed tumor growth in C3H/HeN mice, but not in Toll-like receptor 4 (TLR4)-mutant C3H/HeJ mice, by reducing serum levels of IL-17 and IL-23, while increasing interferon (IFN)-γ levels. The antitumor activity and IFN-γ production were mediated by T cells. Moreover, in vitro experiments showed that Spirulina LPS impaired the antigen-presenting function that supports the generation of IL-17-producing cells in a toll-like receptor (TLR)4-dependent manner. Of note, injection of anti-IL-17 antibody in tumor-bearing C3H/HeN mice in the absence of Spirulina LPS markedly suppressed tumor growth and augmented IFN-γ responses. Thus, our results support the notion that IFN-γ and IL-17/IL-23 mutually regulate Th17 and Th1 responses in tumor-bearing hosts, and Spirulina LPS modulates the balance of the IFN-γ-IL-17/IL-23 axis towards IFN-γ production, which leads to tumor inhibition. Furthermore, Spirulina LPS effectively inhibited the spontaneous development of mammary tumors. This study has important implications for the exploitation of TLR-based immunomodulators for cancer immunotherapy.
Introduction
Although the immune system generally recognizes abnormal proteins on tumor cells as tumor antigens, spontaneous immune responses are too weak to suppress tumor growth. To overcome this problem, a variety of adjuvants, including toll-like receptor (TLR) ligands, are investigated to potentiate antitumor immunity. The bacillus Calmette-Guérin (BCG), historically known for its effective adjuvant properties, is often used in the treatment of cancer patients (1).
The innate immune system recognizes pathogen-associated molecular patterns expressed on microorganisms through corresponding TLRs, and the activation of innate immunity by TLRs produces proinflammatory cytokines such as interleukin (IL)-6 and IL-12, leading to the subsequent induction of adaptive immune responses (2,3). IL-12 is produced by macrophages (MΦ) and dendritic cells (DC) and dictates the differentiation of CD4 Th1 cells, which produce interferon (IFN)-γ and activate natural killer (NK) cells and cytotoxic CD8 T cells (4). IFN-γ plays an important role in the prevention of primary tumor development and intracellular pathogen invasion (5–7). Among the different TLR ligands, lipopolysaccharide (LPS) from gram-negative bacteria exhibits antitumor activity in addition to marked toxicity (8). The study of the bioactivity of LPS from various species revealed that LPS prepared from Bordetella pertussis and a synthetic analog of the LPS lipid A subunit are less toxic than E. coli LPS, and display antitumor effects (9,10).
Recent studies have revealed that IL-23/IL-17 signaling plays an important role in tumorigenesis and metastasis in humans and in mice (11–16). IL-17 is primarily produced by T cells and acts on tumor cells and tumor-associated stromal cells to induce angiogenesis and the production of IL-6, IL-8, and matrix metalloproteinases. IL-23 is produced by Mϕ/DC and facilitates the expansion and survival of IL-17-producing CD4 T (Th17) cells and therefore, the production of IL-17 (17,18). Moreover, it has become evident that a combination of IL-6 and transforming growth factor (TGF)-β induces Th17 differentiation from naive T cells (19,20). Since Mϕ/DC produces both antitumor (IL-12) and tumor-promoting (IL-6/IL-23) cytokines upon stimulation with TLR ligands (21,22), the regulation of this balance is critical for TLR-based cancer immunotherapy (17,18). Moreover, IL-17 stimulates tumor cells and tumor-surrounding cells to induce IL-6 expression, which in turn leads to the activation of signal transducer and activator of transcription 3 (STAT3) (16,23). STAT3 is linked to numerous oncogenic signaling pathways and is constitutively activated both in tumor cells and in immune cells under tumor microenvironment-like conditions. Thus, ideal candidate molecules for tumor immunotherapy are TLR-based immunomodulators that do not induce or partially induce IL-6/IL-23.
While exploring TLR4 responsiveness of the material extracted from algae and cyanobacteria (24), we found that LPS phenol-water extracts from Spirulina (Arthrospira) were able to induce IL-12. Noteworthy, Spirulina LPS showed a much lower in vitro induction of IL-6 and IL-23 by Mϕ/DC than E. coli LPS. Spirulina is a gram-negative, oxygenic, photosynthetic, filamentous cyanobacterium (blue-green alga), and since the Aztec civilization in Mexico, it has been widely used as a nutritional and therapeutic supplement (25). Spirulina LPS is reported to be less toxic compared to LPS from Salmonella abortus (26), but its effects on cytokine production or antitumor activities have not been studied extensively. Thus, it would be very interesting to study how Spirulina LPS affects tumor growth and in vivo production of inflammatory cytokines.
Although most experiments examined the in vitro production of IL-17-associated inflammatory cytokines thus far, the expression patterns of these cytokines in tumor host tissue remain to be established. We report here that Spirulina LPS did not induce or only partially induced IL-6 and IL-23 and efficiently suppressed the growth of hepatocellular carcinoma MH134 in a TLR4-dependent manner, by reducing the serum levels of IL-17 and IL-23, while increasing those of IFN-γ. Interestingly, anti-IL-17 monoclonal antibodies (mAb) clearly suppressed tumor growth as efficiently as Spirulina LPS. Furthermore, Spirulina LPS was quite effective in inhibiting spontaneous development of mammary tumors in an oncogene transgenic mouse model.
Hereinfater you will find link to the full paper.
Okuyama H, Tominaga A, Fukuoka S et al. Spirulina lipopolysaccharides inhibit tumor growth in a Toll-like receptor 4-dependent manner by altering the cytokine milieu from interleukin-17/interleukin-23 to interferon-γ Oncology Reports; 2017 Feb; 37(2): 684–694.
Prezentacja antygenu
Prezentacja antygenu – termin obejmujący znaczeniem mechanizmy odpornościowe, które polegają na „ukazaniu” antygenu limfocytom T przy udziale cząsteczek MHC. Głównym celem prezentacji antygenów jest rozwinięcie odpowiedzi swoistej na dany antygen. Charakterystyczne jest to, że antygeny nie są przedstawiane w formie pierwotnej (natywnej), lecz w formie przetworzonej.
Ze względu na zróżnicowanie cząsteczek MHC*, prezentacja antygenu może się przejawiać w jednej z trzech postaci:
*MHC - ang. major histocompatibility complex - główny układ zgodności tkankowej. Stanowi go zespół białek odpowiedzialnych za prezentację antygenów limfocytom T.
- Cząsteczki MHC klasy I, które prezentują antygeny limfocytom Tc (cytotoksycznym), biorą udział w obronie przeciwko patogenom wewnątrzkomórkowym, np. wirusom. Jeżeli taki antygen zostanie rozpoznany jako obcy, komórka prezentująca będzie zabita, jego obecność na cząsteczce MHC klasy I świadczy bowiem o istnieniu patogenu we wnętrzu komórki. Zabijając komórkę, limfocyt Tc zabija zwykle także występującego w niej pasożyta. Można powiedzieć, że w ten sposób jednostka (komórka) jest poświęcana dla dobra ogółu (organizmu).
- Cząsteczki MHC klasy II, które prezentują antygeny limfocytom Th (pomocniczym), nie wywołują śmierci komórki prezentującej antygen. W tym przypadku taka komórka rozpoczyna wydzielanie cytokin, które pobudzają limfocyt Th. Limfocyty Th są istotnymi komórkami regulującymi odpowiedź odpornościową. Dzięki temu cząsteczki MHC klasy II uczestniczą w pobudzeniu innych komórek, za pośrednictwem limfocytów T pomocniczych.
- Prezentacja krzyżowa jest mechanizmem umożliwiającym pobudzenie zarówno limfocytów Th, jak i limfocytów Tc, przy czym biorą w niej udział zarówno cząsteczki MHC klasy I, jak i klasy II. Nie jest to jednak prosta kombinacja dwóch poprzednio wymienionych rodzajów prezentacji antygenu. Zachodzi ona w charakterystyczny sposób z udziałem określonych komórek, które prezentują antygeny jednocześnie na MHC obu klas i nie są zabijane przez limfocyty Tc.
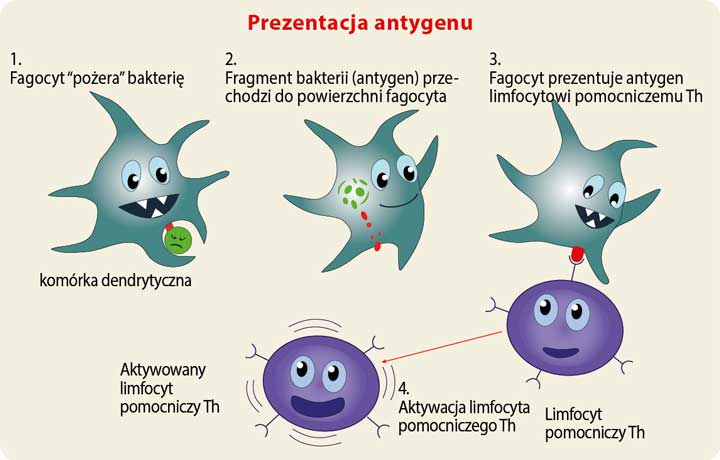
2 Makrofagi i komórki dendrytyczne należą do tzw. komórek prezentujących antygen (Antigen Presenting Cells).
Limfocyty – komórki T i komórki B
Limfocyty należą do krwinek białych (leukocytów) i pochodzą ze szpiku kostnego, ale migrują do różnych części układu limfatycznego, takich jak węzły chłonne, śledzona czy grasica. Są dwa główne rodzaje limfocytów: komórki T i komórki B. Układ limfatyczny obejmuje również system transportowy – układ naczyń limfatycznych – służący do transportu oraz magazynowania limfocytów. Układ limfatyczny zaopatruje/dostarcza limfocyty naszemu organizmowi i odfiltrowuje tkanki z martwych komórek i mikroorganizmów, które nas zaatakowały, takich jak np. bakterie.
Na powierzchni każdego limfocyta znajdują sie receptory, które umożliwiają im rozpoznawanie obcych substancji. Receptory te są bardzo wyspecjalizowane i pasują tylko do jednego swoistego antygenu. Aby to zrozumieć działanie takich specyficznych receptorów pomyślcie o ręce, która może chwycić tylko jeden rodzaj przedmiotu, na przykład tylko jabłko. Taka ręka byłaby prawdziwym mistrzem w chwytaniu jabłek, ale nie byłaby w stanie chwycić cokolwiek innego. W naszym organizmie taki pojedynczy receptor odpowiadałby ręce, która wychwytuje swoje „jabłka”. Limfocyty przemierzają nasz organizm póki nie natrafią na antygen, który ma właściwy kształt i rozmiar pasujący do ich specyficznego receptora. Wydaje się, że może fakt, iż receptory każdego limfocyta mogą pasować tylko do jednego szczególnego rodzaju antygenu będzie stanowił ograniczenie, ale organizm radzi sobie z tym dzięki produkcji takiej mnogości różnorodnych rodzajów limfocytów, że układ odporności jest w stanie rozpoznać niemal każdego intruza.
Limfocyty T
Limfocyty (komórki) T tworzą dwie główne i odmienne grupy: limfocyty pomocnicze T (helper cells) i limfocyty T zabójcy (killer cells). Nazwa limfocyty T pochodzi od łacińskiej nazwy grasicy – thymus – gruczołu położonego za mostkiem. Limfocyty T powstają w szpiku kostnym, następnie migrują do grasicy gdzie dojrzewają.
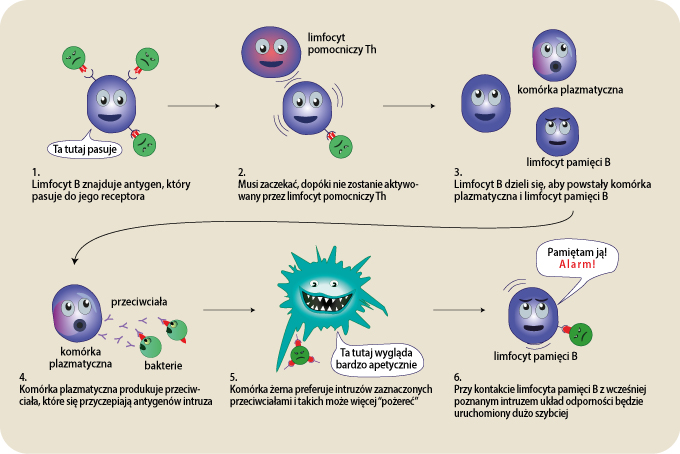
Limfocyty pomocnicze Th (helper) stanowią główną siłę napędową i regulującą układ odporności. Ich podstawowym zadaniem jest aktywacja limfocytów B oraz limfocytów T zabójców. Jednak limfocyty pomocnicze Th same muszą być wcześniej aktywowane. Dzieje się to wówczas, gdy makrofag lub komórka dendrytyczna, która wcześniej pochłonęła intruza, przemieści się do pobliskiego węzła chłonnego i zaprezentuje informację o załapanym patogenie. Komórka żerna (fagocyt) przedstawia fragment antygenu intruza na swej powierzchni w procesie znanym prezentacją antygenu. Limfocyt pomocniczy Th zostaje aktywowany, gdy jego receptor rozpozna antygen. Raz aktywowany limfocyt pomocniczy Th zaczyna się dzielić i produkować białka, które aktywują limfocyty B i T jak również inne komórki układu odporności.
Limfocyt T zabójca (killer cell) jest wyspecjalizowany w atakowaniu komórek organizmu zakażonych wirusami, a czasem bakteriami. Atakuje również komórki raka. Limfocyt T zabójca posiada receptory do wyszukiwania każdej komórki, która pasuje. Komórka, jeśli jest zakażona, jest szybko zabijana. Zakażone komórki są rozpoznawane dzięki drobnym śladom intruza - antygenowi, który może być wykryty na ich powierzchni.
Limfocyty B
Limfocyt B poszukuje antygenu pasującego do jego receptorów. Jeśli znajdzie taki antygen to przyłączy się do niego i wewnątrz limfocyta B jest uruchamiany sygnał spustowy. Ale żeby zostać w pełni aktywowanym, limfocyt B potrzebuje jeszcze białka produkowanego przez limfocyty pomocnicze Th. Gdy to nastąpi limfocyt B zaczyna się dzielić produkując swoje klony komórkowe i w czasie tego procesu powstają dwa nowe typy komórek: komórki plazmatyczne i limfocyty pamięci B.
Komórka plazmatyczna jest wyspecjalizowana w produkcji swoistych białek zwanych przeciwciałami, które będą oddziaływać na taki antygen, który pasuje do receptora limfocyta B. Przeciwciała uwalniane przez komórki plazmatyczne potrafią wyszukać „intruzów” i pomóc w ich zniszczeniu. Komórki plazmatyczne produkują przeciwciała w niezwykłym tempie i potrafią uwalniać dziesiątki tysięcy przeciwciał na sekundę. Gdy Y-kształtne przeciwciała napotkają pasujący antygen, przyłączają się do niego. Przyłączone przeciwciała służą jako „smakowita otoczka” dla komórek żernych, takich jak makrofagi. Przeciwciała neutralizują również toksyny i unieszkodliwiają wirusy, zapobiegając zakażaniu przez nie nowych komórek. Każde ramię Y-kształtnego przeciwciała może przyłączyć się do różnego antygenu. Tak więc gdy jedno ramię łączy się z jednym antygenem na jednej komórce, to drugie ramie może przyłączać się do innej komórki. W ten sposób patogeny są zbierane w większe grupy, które łatwiej jest sfagocytować komórkom żernym. Poza tym bakterie i inne patogeny pokryte przeciwciałami są łatwiejszym celem na atak białek układu dopełniacza.
Limfocyty pamięci B (komórki pamięci B) są drugim rodzajem komórek produkowanych przez kategorię limfocytów B. Komórki te mają wydłużony okres życia i dlatego mogą „pamiętać” swoistych intruzów. Również kategoria limfocytów T może produkować komórki pamięci, mają one nawet dłuższy okres życia niż limfocyty B pamięci. Gdy intruz próbuje powtórnie zaatakować organizm, to limfocyty pamięci B oraz T, które już go znają, pomagają aktywować układ odporności znacznie szybciej. Najeźdźcy zostają wprost “wymieceni”, zanim zakażona osoba poczuje jakiekolwiek objawy. Organizm został uodporniony na intruza.
Aktywacja limfocytów pamięci B